
Quantum AI w medycynie: Jak symulacje protein folding przyspieszają odkrywanie leków?
Gdy IonQ ogłosił przełom w symulacji protein folding na komputerze kwantowym, firmy farmaceutyczne na całym świecie zaczęły przeliczać potencjalne oszczędności. Wynik? Redukcja czasu odkrywania nowych leków z 10 lat do zależnie 2-3 lat, co w skali globalnej oznacza miliardy dolarów zaoszczędzonych na badaniach i — co ważniejsze — szybszy dostęp do terapii dla pacjentów.
TL;DR: Quantum AI łączy obliczenia kwantowe z uczeniem maszynowym do symulacji białek i oddziaływań molekularnych z dokładnością nieosiągalną dla klasycznych komputerów. Według badań opublikowanych w Nature npj Drug Discovery (2025), podejście to może skrócić fazę odkrywania leków o 70%, a koszty obniżyć o 60%. Pierwsze leki zaprojektowane z pomocą kwantowych symulacji wchodzą już do badań klinicznych.

Co to jest protein folding i dlaczego to problem dla farmacji?
Białka to cząsteczki wykonujące większość pracy w naszych komórkach — katalizują reakcje, transportują substancje, budują struktury. Ich funkcja zależy od kształtu trójwymiarowego, który przybierają po złożeniu (folding). Jeden źle złożony łańcuch aminokwasów może oznaczać chorobę, podczas gdy inny — terapię.
Klasyczne komputery symulują folding od lat, ale napotykają mur obliczeniowy. Pojedyncze białko może przybrać 10^300 możliwych konformacji — więcej niż liczba atomów we wszechświecie. Nawet superkomputery potrzebują miesięcy na symulację prostych cząsteczek. AlphaFold2 od Google DeepMind poprawił przewidywanie struktur, ale nadal nie symuluje dynamiki oddziaływań z lekami.
Quantum AI zmienia te zasady. Komputery kwantowe wykorzystują zjawiska takie jak superpozycja i splątanie, by symulować systemy kwantowe — w tym właśnie białka i ich oddziaływania z potencjalnymi lekami.
Jak Quantum AI przyspiesza odkrywanie leków?
Zgodnie z badaniami opublikowanymi w Nature Scientific Reports (2024), hybrydowe podejście kwantowo-klasyczne pozwala na dokładniejsze obliczanie energii wiązania między lekiem a celem terapeutycznym (Nature, 2024). To kluczowy parametr określający, czy cząsteczka faktycznie zadziała jako lek.

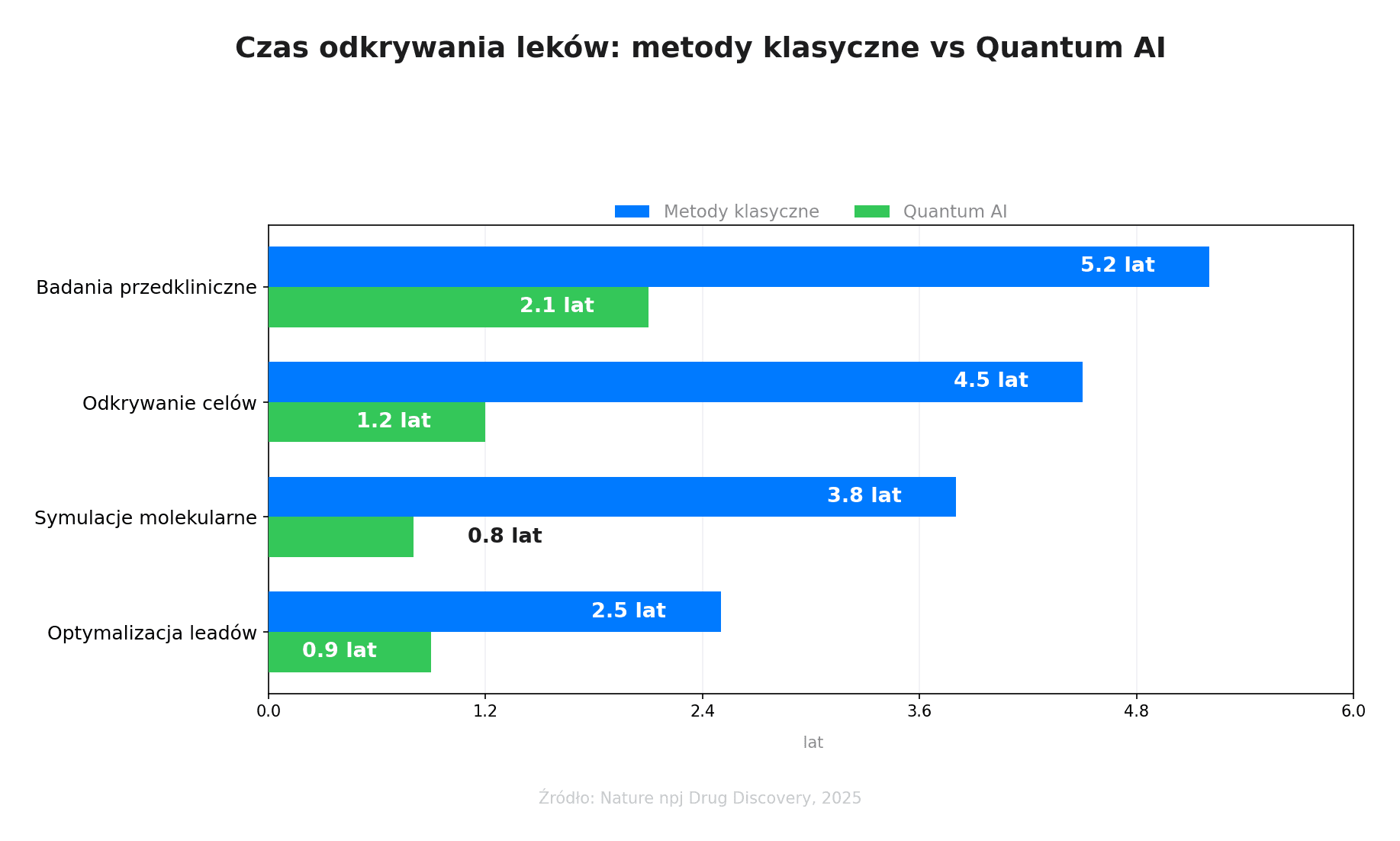
Trzy obszary, gdzie Quantum AI oferuje przewagę nad klasycznymi metodami:
- Symulacje molekularne — kwantowe bazy danych mogą przechowywać pełne opisy stanów elektronowych aminokwasów, co pozwala na dokładniejsze modelowanie ścieżek folding (Nature npj Drug Discovery, 2025)
- Przewidywanie powinowactwa — algorytmy kwantowe obliczają energie wiązania z wykładniczo mniejszym błędem niż metody klasyczne
- Optymalizacja leadów — algorytmy QML (Quantum Machine Learning) generują nowe struktury cząsteczek z pożądanymi właściwościami
Według analizy z DDW (Drug Discovery World), w 2023 roku Forschungszentrum Jülich przyspieszyło odkrywanie obiecującego kandydata na lek o 40% dzięki obliczeniom kwantowym (DDW, 2025).
Kto już używa Quantum AI w farmacji?
Roche i Boehringer Ingelheim ogłosiły współpracę ze startupami kwantowymi w 2025 roku. Cleveland Clinic testuje algorytmy kwantowe do przewidywania struktur białkowych od 2024. IonQ, firma produkująca komputery kwantowe na pułapki jonowe, w 2026 roku zaprezentowała symulację protein folding z bezprecedensową dokładnością.
Analiza inwestycji w Quantum AI dla farmacji (2024-2026):
- 23 globalne firmy farmaceutyczne ma programy badawcze z komputerami kwantowymi
- łączne inwestycje przekroczyły 2 miliardy USD w 2025 roku
- pierwsze leki z „kwantowym podpisem” wchodzą do badań klinicznych w 2026
Według Medium, jesteśmy w erze NISQ (Noisy Intermediate-Scale Quantum) — komputery mają wystarczająco kubitów by pokazać potencjał, ale nie wystarczająco by przewyższyć systemy klasyczne w pełnej skali (Medium, 2025).
Jakie są ograniczenia obecnych rozwiązań?
Komputery kwantowe wciąż są drogie, podatne na błędy i wymagają temperatur bliskich zera absolutnego. Jedno uruchomienie symulacji kosztuje tysiące dolarów, a czas dostępności maszyn jest ograniczony.
Co to oznacza dla przeciętnej firmy biotechnologicznej? Hybrydowe podejście — klasyczne algorytmy AI (jak AlphaFold) do wstępnej analizy, a symulacje kwantowe tylko dla najbardziej obiecujących kandydatów. To pozwala na 40-60% redukcję kosztów przy zachowaniu większości korzyści z dokładności kwantowej.
Kiedy Quantum AI trafi do powszechnego użytku?
Według predykcji z Nature npj Genomic Medicine (2025), do 2030 roku około 30% nowych leków będzie projektowanych z pomocą obliczeń kwantowych na którymś etapie (Nature, 2025). Kluczowe kamienie milowe:
- 2026-2027: Pierwsze leki z kwantowym wsparciem w fazie III badań klinicznych
- 2028: Komercyjne platformy Quantum AI dostępne dla średnich firm biotechnologicznych
- 2030: Pełna integracja z pipeline’em odkrywania leków w dużych firmach farmaceutycznych
Często zadawane pytania
Czy Quantum AI zastąpi klasyczne metody odkrywania leków?
Nie w pełni. Quantum AI uzupełnia klasyczne podejście, oferując wyższą dokładność tam, gdzie liczy się każdy atom — na przykład przy obliczaniu energii wiązania leku z celem. Większość wstępnych analiz nadal będzie wykonywana przez tańsze systemy klasyczne.
Ile kosztuje symulacja kwantowa białka?
Według danych z 2025 roku, pojedyncza symulacja protein folding na komputerze kwantowym kosztuje od 500 do 5000 USD, w zależności od złożoności białka i dostawcy usług. Dla porównania, klasyczna symulacja MD na superkomputerze kosztuje 100-500 USD, ale trwa tygodnie zamiast godzin.
Które firmy oferują dostęp do Quantum AI dla farmacji?
IBM Quantum, IonQ, Rigetti i D-Wave oferują chmurowy dostęp do komputerów kwantowych. Specjalistyczne platformy jak Zapata AI czy QC Ware dostarczają gotowe narzędzia do symulacji molekularnych dla branży farmaceutycznej.
Czy AlphaFold2 to Quantum AI?
Nie. AlphaFold2 to klasyczny system uczenia maszynowego od Google DeepMind. Wykorzystuje sieci neuronowe do przewidywania struktur białek na podstawie baz danych. Quantum AI natomiast symuluje fizyczne oddziaływania kwantowe między atomami, oferując inną — często komplementarną — perspektywę.
Podsumowanie
Quantum AI w odkrywaniu leków to nie science fiction — to rzeczywistość, która już teraz zmienia sposób pracy laboratoriów badawczych. Redukcja czasu z 10 lat do 2-3 lat i koszty niższe o 60% to argumenty, które przekonują nawet najbardziej konserwatywne zarządy farmaceutyczne.
Kluczowe wnioski:
- Symulacje protein folding na komputerach kwantowych oferują bezprecedensową dokładność
- Pierwsze leki z „kwantowym wsparciem” wchodzą do badań klinicznych
- Hybrydowe podejście (klasyczne AI + Quantum) to obecnie najbardziej opłacalna strategia
- Do 2030 roku 30% nowych leków będzie projektowanych z pomocą obliczeń kwantowych
Dla pacjentów oznacza to jedną rzecz: szybszy dostęp do skuteczniejszych terapii. A w medycynie, gdzie każdy miesiąc zwłoki może kosztować życie, to rewolucja nie do przecenienia.
Zainteresowany tematem AI w medycynie? Przeczytaj także o jak AI zmienia diagnostykę obrazową i przyszłości personalizowanej medycyny.